1. 서 론
2. 실험 방법 및 재료
2.1 실험 재료
2.2 실험 방법
3. 실험 결과 및 고찰
3.1 생존량 평가
3.2 생물축적량 평가
3.3 수중용출량 분석
3.4 공극수 농도 분석
4. 결 론
1. 서 론
퇴적토는 장기적 관점으로 보았을 때, 영양분의 균형, 하 천의 건강성 등에도 큰 영향범위를 가지는 만큼 오염된 퇴적토의 관리는 지속 가능한 개발뿐 아니라 전체 수생태계를 위해서도 매우 중요한 관리자원이다(Yan & Li, 2023). 오염된 퇴적토를 제거하기 위해 준설 공법이 이용되고 있지만 준설 과정에서 안정화되어있던 오염물질의 유출 가능성이 있고(Hong et al., 2023), 준설에 의한 재 부유 및 침전에 의한 2차 영향을 초래할 수 있다(Harwood et al., 2022). 오염 퇴적토 위에 모래물질, 개량제 등을 이용해 안정화층, 격리층, 필터층을 구성하는 캡핑 또한 오염 퇴적토의 관리 방법 중 한 가지로 거론되고 있다(Mohan et al., 2000). 저비용 공정과 친환경적인 특성이 장점이지만, 균질성 유지의 어려움과 퇴적량의 증가로 인한 한계가 존재한다(Vandenbossche et al., 2015). 이러한 방법의 대안으로 안정화가 주목받고 있으며(Choi et al., 2016), 활성탄의 흡착을 이용한 퇴적토 내 유기오염물질의 안정화가 많은 주목을 받고 있다(Abel & Akkanen., 2019; Nasrullah et al., 2018; Zhao et al., 2023).
활성탄의 흡착은 표면에 존재하는 다양한 표면작용기와 기공의 크기 등에 의해 발생하며(Srivastava et al., 2021), 활성탄을 산/염기를 이용하여 개질할 시, 표면 반응성이 높은 다공성 물질인 활성탄의 표면 작용기의 양과 다양성을 증가시켜 흡착량을 증가시킬 수 있다. HNO3를 이용한 개질을 통해 카르보닐기, 카르복실기, 페놀기 및 락톤기의 양이 증가하였다. 산/염기를 이용하여 활성탄 개질을 진행한 후 비표면적의 변화는 2% 미만을 나타내었으며, 카르복실기의 함량이 최대 14.3% 증가한 결과를 확인하였다(Kim et al., 2012). 또한 산/염기로 활성탄의 개질 진행 후 Energy-dispersive X-ray spectroscopy(EDS) 분석결과 28wt% 이상의 산소함량을 가진 것을 확인하였으며, 개질 전 대비 두 배 이상의 산소함량이 늘었으며, 그 조성의 대부분이 카르복실기 및 기타 산소그룹이었다(Kim et al., 2014).
퇴적토와 개질된 활성탄을 혼합한 후 폴리옥시메틸렌(Polyoxymethylene)을 채취기로 이용하여 안정화 정도를 측정한 결과, 오염퇴적토에 존재하는 공극수의 유기오염물질을 장기간 흡착할 수 있었다(Oen et al., 2012). 활성탄이 저서생물에 미치는 영향의 연구 결과, Lumbriculus variegatus에 유의미한 영향을 미치지만, 생존에 직접적인 영향을 미치는 결과는 확인하지 못하였다는 결과를 나타내었다(Yates et al., 2023). 다만, 다량의 활성탄을 퇴적토에 흡착제로 이용 시, 수생태계에 영향을 미칠수도 있기에 이에 대한 고려도 필요하다(Yates et al., 2023).
기존 연구에서 혼합된 개질활성탄을 사용하여 퇴적토의 공극수 안정화, 용출수 안정화, 저서생물에 미치는 영향을 종합적으로 진행한 연구 결과는 아직 확인되지 않았다. 프탈레이트 중 Benzyl butyl phthalate(BBP)는 플라스틱의 가소제로 사용되며, 플라스틱과 공유결합을 이루고 있지 않기에 환경으로 침출되어 수생 생태계에 부정적인 영향을 미치고 있다(Paquette et al., 2024). 따라서 본 연구에서는 산/염기 개질활성탄을 이용하여 퇴적토에 축적되어있는 유기오염물질 안정화 공정을 연구하였으며, 저서생물을 이용한 유기오염물질의 저감 및 활동에 의한 안정화 과정과 수층으로 용출되는 유기오염물질의 안정화 양을 연구하였고, 유기오염물질 중 BBP를 대표 물질로 선정하였다.
2. 실험 방법 및 재료
2.1 실험 재료
2.1.1 안정화제 합성
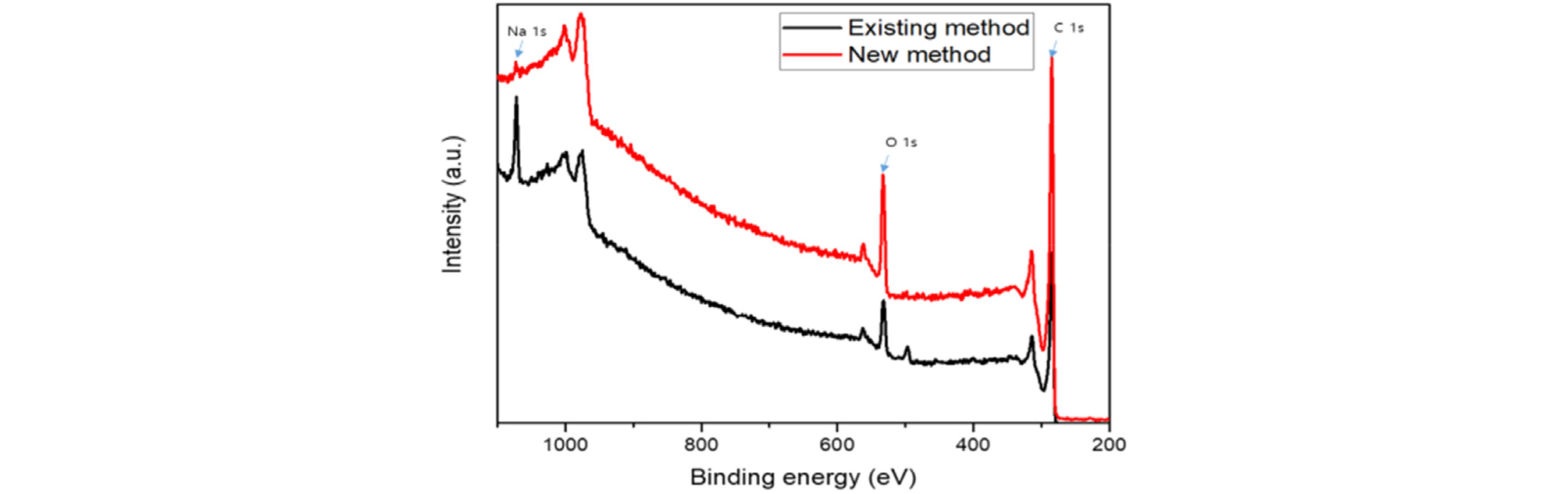
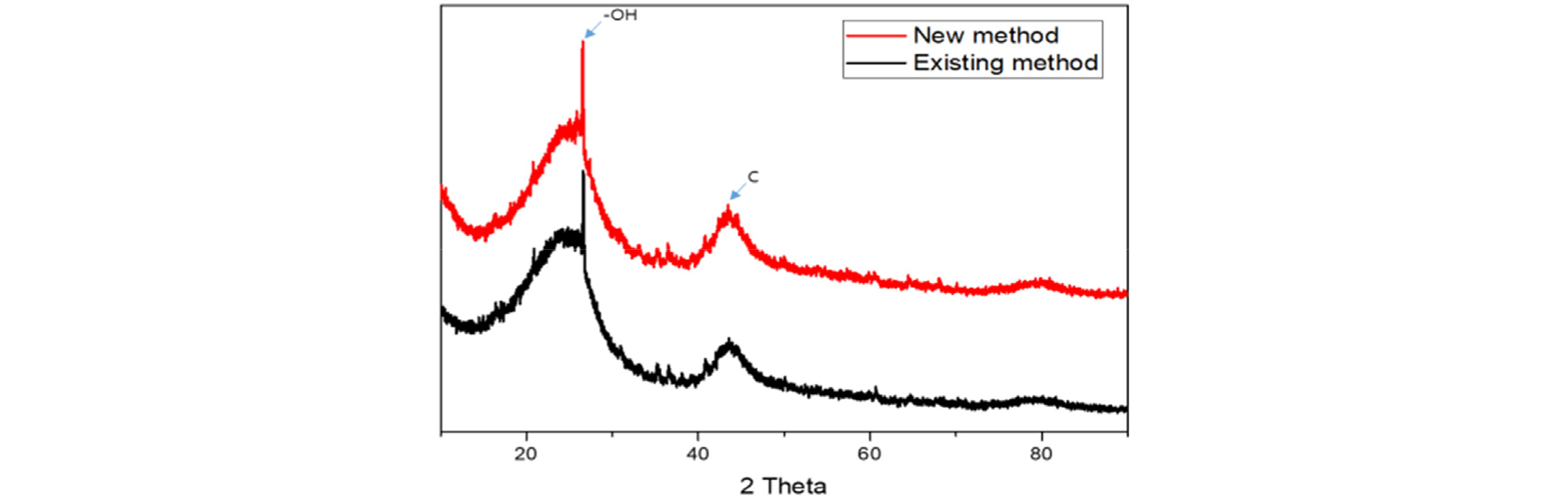
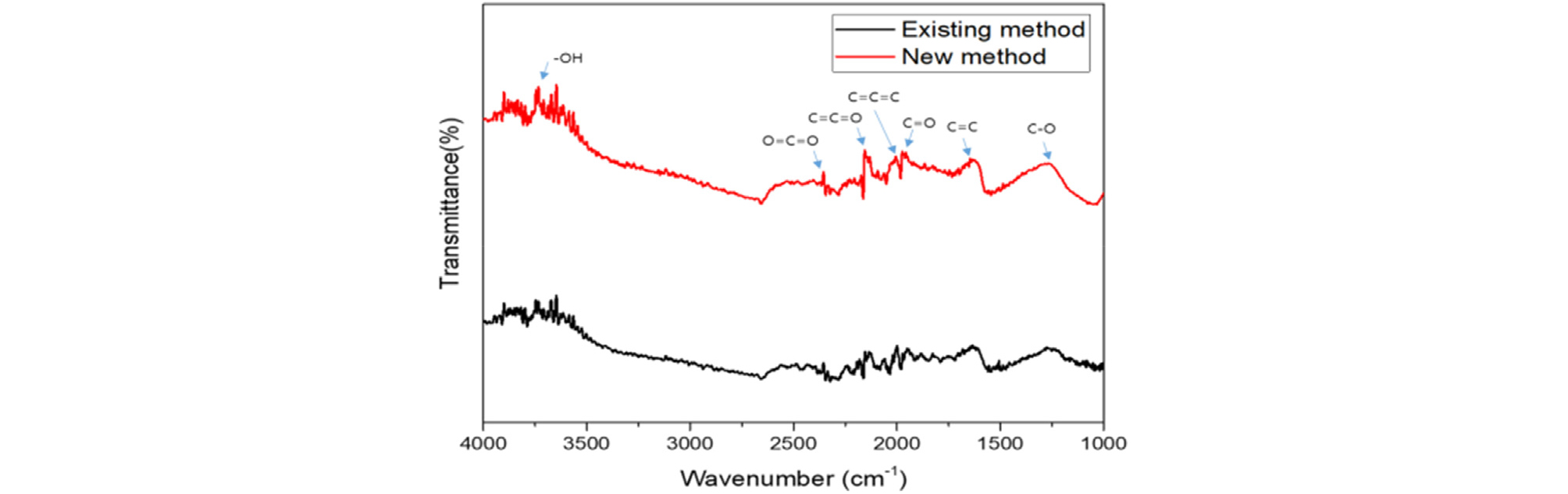
기존 개질 방법(Existing method)(Kim et al., 2012) 을 이용하여 활성탄의 개질 진행 시, 그 양이 소량이었다. 이를 개선하고자 개질 방법을 일부 수정하여 대용량 개질 방법(New method)으로 진행하였다. 이를 통해 1L당 12g을 개질할 수 있었던 기존 개질방법보다 10배 더 많은 120g을 개질할 수 있었으며, 약 130분의 소요 시간을 90분으로 단축할 수 있었다. 기존의 방법을 이용한 활성탄과의 물성 차이를 확인하기 위해 분석을 진행하였다. C사에서 구매한 HNO3 298.01mL를 2L 플라스크에 담은 후 Y사의 Basic360serise 증류장치를 이용하여 생산된 2차 증류수로 표선을 맞추어 70%, 5M 농도의 질산 용액을 제조한다. C사에서 구매한 활성탄을 갈아서 75μm 크기로 채반에 걸러준다. 질산 용액에 활성탄 240g을 넣고 2시간 교반한다. S사에서 구매한 NaOH 8g을 2L 플라스크에 담은 후 2차 증류수로 표선을 맞춘 뒤 2시간 교반하여 0.1M 농도의 NaOH 용액을 제조한다. 질산 용액과 활성탄을 혼합한 용액을 진공필터를 이용하여 활성탄과 질산 용액을 분리한다. 진공필터(φ = 70mm)는 W사의 필터를 이용하였다. 분리된 활성탄에 제조한 0.1M 농도의 NaOH 용액을 혼합한 후 질산 용액 분리 과정과 동일한 조건으로 2회 반복한다. 2회 반복을 마친 활성탄을 2차 증류수에 혼합하여 질산 용액 분리과정과 동일한 조건으로 1회 진공분리를 진행한다. 2차 증류수와 활성탄을 분리한 후, 도가니에 옮겨담아 H사의 건조기에 80℃ 조건으로 24시간 건조한다. 두 활성탄의 물성 분석을 위해 기기분석을 진행하였고, X-ray photoelectron spectroscopy(XPS), X-ray diffraction(XRD), Brunauer emmett teller(BET), Fourier transform infrared(FT-IR), Zeta potential을 이용하여 분석하고 Fig. 1, Fig. 2, Fig. 3, Table 1, Table 2에 나타내었다.
Table 1.
BET results of the modified activated carbon
| Existing capacity modified | New capacity modified | |
| BET Surface Area (m2/g) | 972 | 1,011 |
| Pore Volume (m3/g) | 0.68 | 0.707 |
| Pore Size (nm) | 2.13 | 2.13 |
Table 2.
Zeta potential of the modified activated carbon
|
Zeta Potential (mV) | Existing capacity modified | New capacity modified |
| -32.5 | -23.5 |
기존 개질방법을 이용한 개질활성탄과 대용량 개질방법을 이용한 개질활성탄을 XPS 분석장비를 이용하여 peak 측정을 통한 활성탄에 결합된 작용기를 분석하였다. 분석결과, 기존 개질방법을 이용한 개질활성탄과 대용량 개질방법을 이용한 개질활성탄 모두 1,072eV 부근에서 Na 1s peak, 532eV 부근에서 O 1s peak, 284eV 부근에서 C 1s peak이 관측되었다. XRD 분석결과, 두 개질활성탄 모두 OH와 C에 해당하는 peak이 동일하게 관찰되었고, 두 그래프의 유사도가 매우 높게 나타났으며, BET를 이용한 물성분석 결과 대용량 개질방법을 이용한 경우, 기존 개질방법을 이용한 경우보다 39m2/g 더 큰 surface area 값과, 0.027m3/g 더 큰 pore volume 값을 보였고, pore size는 2.13nm로 동일한 수치를 보였다. 기존 개질방법과 대용량 개질방법을 이용한 두 활성탄의 FT-IR 그래프 분석 결과, 3,700-3,200cm-1 범위에서 -OH, 2,349cm-1에서 O=C=O, 2150cm-1에서 C=C=O 등 두 개질활성탄 모두 동일한 peak이 측정되었으며, 그래프의 형상이 높은 유사도를 보였다. Zeta potential을 이용한 두 활성탄의 물성 비교·분석 결과, 두 개질방법 모두 음의 표면전위를 가지고 있어 카르복실기와 수산화기 등의 작용기의 형성이 발생했을 것이며, 9mV의 표면전하 차이를 발견하였으나 개질방법의 차이에 따른 유의미한 수준의 표면전하로 판단하기는 어렵다. 기존 개질방법을 이용한 개질활성탄과 대용량 개질방법을 이용한 개질활성탄의 분석기기를 통한 물성 특성 비교 결과, 목표하고자 하는 작용기의 형성과 비표면적의 증가에 따른 유의미한 차이점이 발견되지 않았기에, 대용량 개질방법을 이용하여 합성한 안정화제를 실험에 사용하였다.
2.1.2 Low-density polyethylene(LDPE) 수동 샘플러 제작
유기오염물질의 측정을 위해 LDPE 필름을 사용하였다. 지름 5.5cm의 원형과 2.5cm × 15cm(가로 × 세로)로 LDPE를 자른 후 세척을 진행하였다. 세척은 광구병에 D사의 순도 99.5% 헥산과 LDPE를 혼합하여 뚜껑을 닫은 후 교반기를 이용하여 상온에서 24시간 교반한 후 LDPE는 남겨두고 헥산은 따라낸 뒤, 같은 광구병에 S사에서 구입한 아세톤에 혼합하여 오비탈 셰이커에 3시간 교반한다. 교반을 마친 광구병을 꺼내어 아세톤을 따라낸 후, LDPE를 2차 증류수에 3회 세척하고, H사의 건조기를 이용하여 60℃ 온도에 24시간 건조한다. 세척을 마친 LDPE는 한 개의 클립에 2cm 간격으로 2개를 감고, 원형의 LDPE는 3장을 겹쳐서 클립을 삼발이 형태로 꼽아 수동 샘플러로 이용한다.
2.1.3 OECD water 제조
본 실험에 이용된 물은 실제 담수를 모사한 용액인 OECD water를 사용하였다. 제작 방법은 용액 1L 기준 2차 증류수 1L, CaCl2·2H2O 11.76g, MgSO4·7H2O 4.93g, NaHCO3 2.59g, KCl 0.23g을 1L 부피 플라스크에 넣고 24시간 교반하여 제작한다. 본 실험에서는 제작한 OECD water 용액을 40배 희석하고 1일 이상 폭기하여 사용하였다.
2.1.4 Lumbriculus variegatus
본 실험에 저서생물로 이용되는 생물은 실험실에서 배양이 가능한 수준의 환경 민감도, 빠른 번식주기(Mount et al., 2006), 높은 독성 민감도를 가지고 기존의 독성자료가 많아 비교가 수월하며 생물혼합 및 생물 영향평가를 위하여 대중적으로 이용되는 Lumbriculus variegatus 를 이용한다. 실험에 이용되기 전, 20±0.5℃의 배양 온도, 16/8시간의 광주기, 일주일에 3회 OECD water로 환수 및 먹이를 공급하며 상시 폭기 상태의 서식 환경을 조성하였다.
2.2 실험 방법
2.2.1 Microcosm 실험
지름 6cm, 높이 15cm 원통형으로 된 유리 소재의 microcosm 용기를 실험에 이용한다. 용기 내부의 물질 유출을 방지하기 위해 하단부 마개에 테프론 테이프를 3회 감은 뒤 microcosm에 끼우고 외부를 파라필름으로 2회 감는다. 실험에 이용되는 퇴적토는 대한민국 안동시 안동댐의 퇴적토를 건조 후 사용하였다. 건조는 H사의 HST-502M 건조기를 사용하여 80℃에 6시간 이상 건조 후 2mm 크기의 입자를 이용하기 위해 채반을 사용하여 분리하였다. 상단에 건조된 퇴적토를 투하 후 흔들어서 분류하고 500mL 광구병에 200g을 채취하여 옮겨 담았다. 인공오염을 위해 S사에서 구입한 순도 98% BBP를 S사에서 구입한 아세톤 250mL와 혼합하여 녹인 뒤, 퇴적토를 옮겨 담은 광구병에 붓고 뚜껑을 닫아 후드 안에서 교반기로 24시간 교반한다. 뚜껑을 열어 3시간 동안 아세톤이 증발하도록 한 뒤, 샬레에 옮겨 담고 후드 안에서 24시간 동안 자연건조 시킨다. 완전 건조된 오염토를 퇴적토 1,333g과 혼합 후 혼합기를 이용하여 24시간 혼합하여 0.3mg/L의 농도로 BBP에 오염된 퇴적토(concentration sediment)를 실험에 이용하였다.
실제 환경과 유사한 환경을 lab-scale로 모사하기 위해 오염 퇴적토 8cm와 OECD water 250mL를 붓고 24시간 안정화 기간을 거친 후 Lumbriculus variegatus 20마리를 넣어 control을 제작하였다. Lumbriculus variegatus의 유무에 따른 영향을 확인하기 위해 control에서 Lumbriculus variegatus를 제외한 실험군을 제작하였다. 안정화제의 혼합방법과 혼합비율에 따른 안정화 양을 평가하기 위한 실험군을 구성하였다. 퇴적토 부피 대비 5%, 10%의 안정화제를 혼합한 두 항목과 전체 토양 8cm를 혼합한 기계혼합(Mechanical mixing), 생물에 의한 혼합을 확인하기 위해 6cm의 퇴적토와 그 위 2cm는 안정화제를 혼합한 혼합토를 덮은 생물혼합(Bio mixing) 총 5개의 실험군을 구성하였다. 모든 실험군에는 OECD water 250mL를 넣고 24시간 안정화 기간을 거친 후, LDPE 필름을 감은 클립을 토양의 바닥과 표면으로부터 1cm, 클립의 간격은 2cm로 하여 총 2개의 클립을 토양에 삽입하고 원형 LDPE 필름을 설치한 후 Lumbriculus variegatus를 20마리 투입하였다. 표층수의 증발을 방지하기 위해 microcosm 용기를 파라필름으로 덮고 각각의 실험기간에 맞추어(본 실험에서는 7, 14, 21, 28일간 측정) 진행한다. Microcosm의 상등수는 매일 OECD water 30mL를 환수하여 실험을 진행하였다. 제작한 대조군 및 실험군은 아래의 방식으로 지칭하였다.
Table 3.
Experimental set-up in this research
2.2.2 생물 영향평가실험
안정화제의 혼합량에 따른 저서생물 영향평가 실험에 이용하였으며, 생존율과 축적 농도를 분석하였다. 각 microcosm에 20마리의 Lumbriculus variegatus를 무작위로 투입하고 각 노출 기간별 실험이 종료되면 Lumbriculus variegatus를 꺼내어 생존한 Lumbriculus variegatus의 마리 수를 측정하여 생존율을 평가한다. 꺼낸 Lumbriculus variegatus를 24시간 OECD water에 안정화 후 퇴적토와 수분을 닦아내고 습윤 중량을 측정 후, 건조기를 이용하여 60℃ 온도에 건조 후 동결건조기를 이용하여 -80℃에 동결건조를 진행한다. 동결건조 된 Lumbriculus variegatus의 무게를 측정 후 옥으로 구성된 막자사발을 이용하여 분쇄 후 1:1(v/v) 비율의 헥산과 아세톤 용액 5mL을 추가하고 20분 동안 초음파기기를 이용하여 초음파 처리를 진행한다. 튜브를 원심분리하여 추출하고, 다시 1:1(v/v) 비율의 헥산과 아세톤 용액 5mL을 추가하고 20분 동안 초음파 처리 진행하는 과정을 1회 더 반복한다. 추출된 용액을 M사의 WT-12A 모델 질소농축기를 이용하여 1mL로 농축 후 GC 바이알에 1mL를 옮겨닮고 GC-MS를 이용하여 Lumbriculus variegatus 내부에 존재하는 유기오염물질의 양을 분석한다. 각 실험군 Lumbriculus variegatus의 유기오염물질 양을 안정화제가 혼합되지 않은 control의 결과와 비교하여 안정화 및 Lumbriculus variegatus의 영향을 분석한다.
2.2.3 안정화 측정실험
실험기간에 맞추어 용기 내에 있는 LDPE를 퇴적토에서 분리한다. 이때, 퇴적토의 교란 방지 및 Lumbriculus variegatus 분리의 용이성을 위해 퇴적토 위로 올라오는 Lumbriculus variegatus는 최대한 분리한 후 진행한다. 실험 종료 후 microcosm에서 분리한 원형 LDPE와 클립에 있는 LDPE를 20mL 바이얄에 옮겨 담고 헥산 20mL로 표선을 맞춘다. 24시간 교반 진행 후, 용액과 LDPE를 분리하고 분리한 LDPE에 헥산 20mL을 담고 24시간 교반을 진행한다. 교반을 마친 용액과 미리 분리해 둔 용액을 40mL 바이얄에 옮겨 담고 질소농축기를 이용하여 1mL로 농축한 뒤, GC 바이얄에 옮겨 GC-MS로 분석한다. GC분석이 끝난 후, PE 필름이 있는 20mL 바이얄에서 용매가 완전히 증발하면 집게로 PE를 꺼내어 그 무게를 측정하고 소수점 첫 자리까지 mg 단위로 기록한다.
3. 실험 결과 및 고찰
3.1 생존량 평가
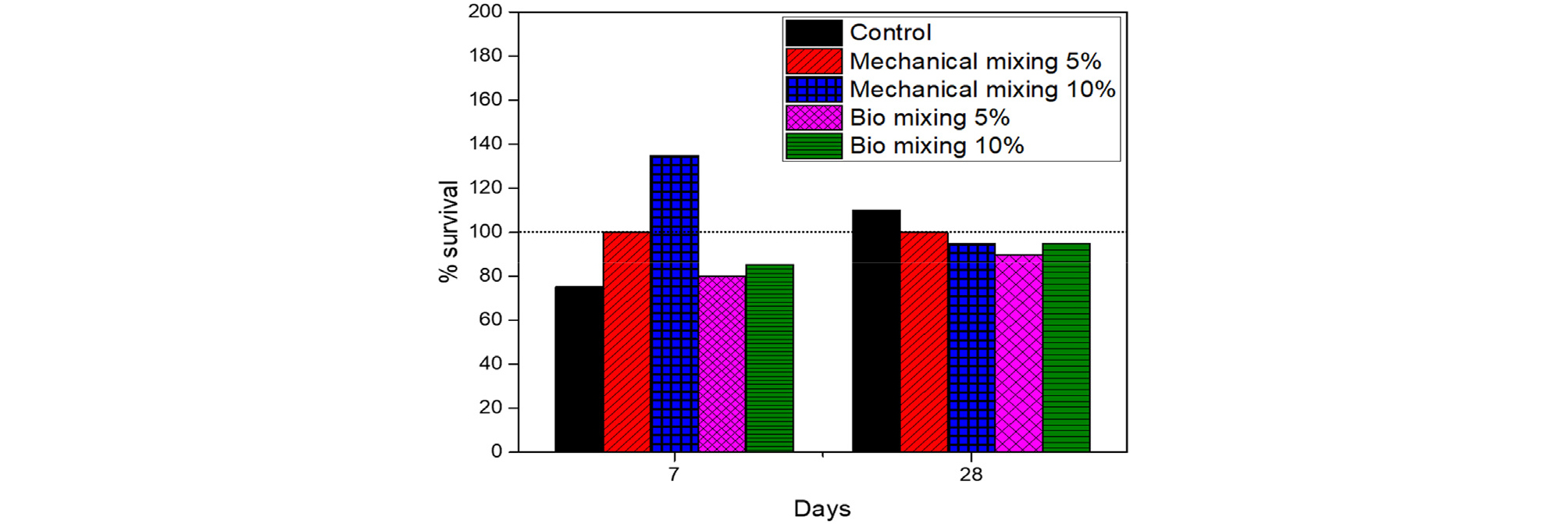
Fig. 4는 7일간 노출된 Lumbriculus variegatus의 생존율과 28일간 노출된 Lumbriculus variegatus의 생존율 결과이다. 모든 실험 조건에서 90% 이상의 생존율을 보였으며, 이는 대체로 안정적인 실험 결과라는 판단을 할 수 있는 근거가 된다(OECD, 2004). 기계혼합 5%의 결과가 가장 변화 없이 안정적인 결과를 보였으며, 생물혼합 10%, 생물혼합 5%, 기계혼합 10%, control 순서로 85~95%, 80~90%, 75~110%, 135~95%의 변화율을 보였다. 생존율은 환경에 대한 차이 등으로 변화할 수 있어 연관성은 찾기 어려우며, 7일차의 Lumbriculus variegatus 생존율과 28일차의 생존율 차이는 활성탄에 의한 어린 Lumbriculus variegatus의 성장 억제 및 사망, 성체 Lumbriculus variegatus의 사망에 의한 수치 감소에 기인한 것으로 판단된다(Yates et al., 2023). 따라서, 개질활성탄의 존재가 Lumbriculus variegatus의 생존량에 영향을 주지 않는다는 판단을 근거로 실험을 진행하였다.
3.2 생물축적량 평가
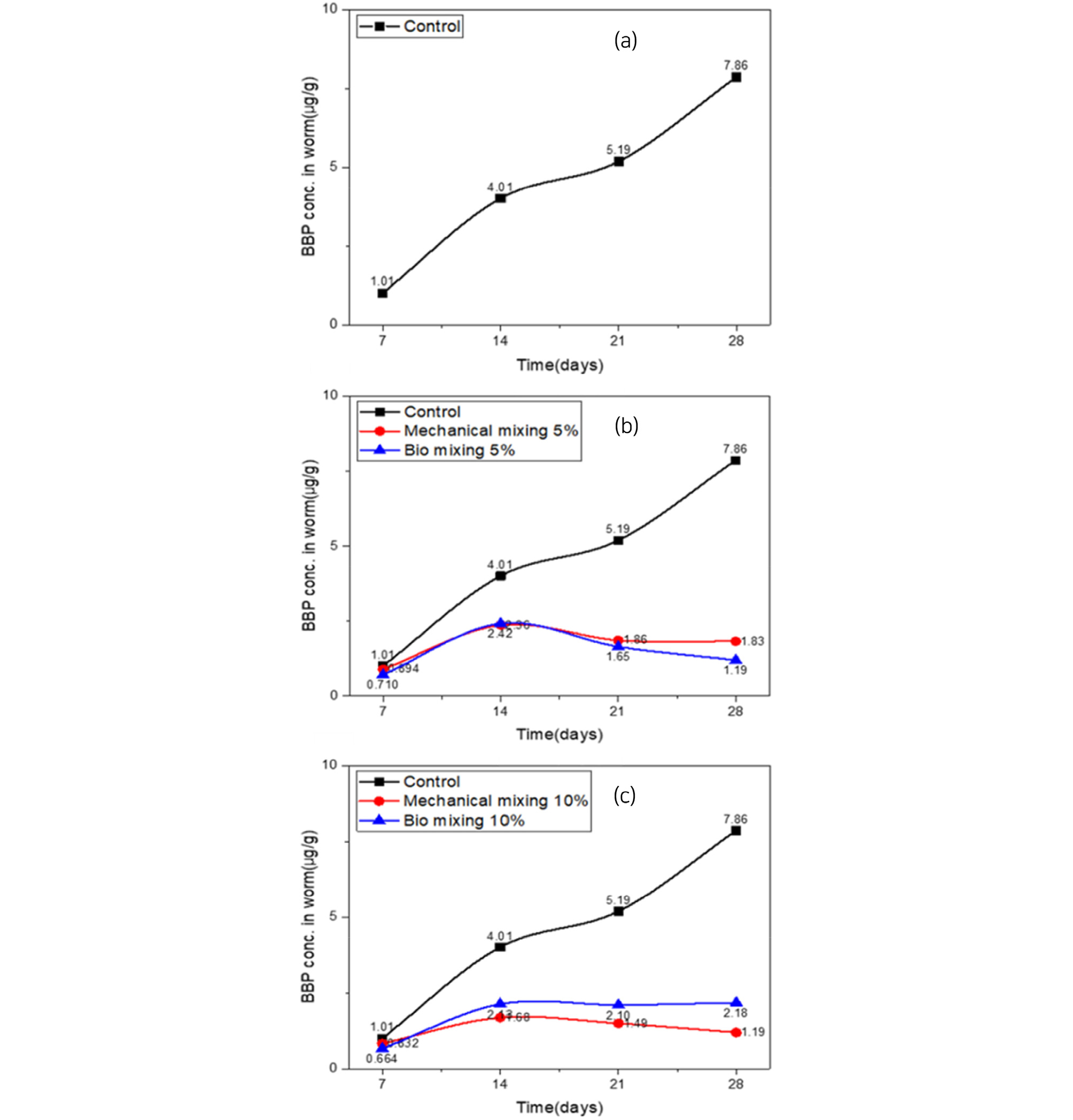
Fig. 5는 개질활성탄 주입 후 28일간 노출시킨 Lumbriculus variegatus에 축적된 유기오염물질의 양을 비교한 결과를 나타내었다. (a)는 control에 존재하는 Lumbriculus variegatus의 채내 BBP 축적량을 나타낸 결과이다. 28일간 Lumbriculus variegatus를 퇴적토에 노출 시킨 후, 일주일 간격으로 Lumbriculus variegatus를 꺼내어 측정한 후 GC-MS를 이용하여 분석하였다. 체내 BBP 축적량은 노출 기간 7일에서부터 28일까지 상승곡선을 나타내며 오염 퇴적토로부터 지속적인 BBP의 영향을 받는 것을 확인할 수 있다. (b)와 (c)는 각각 안정화제의 혼합방법에 따른 체내 축적량을 control과 비교하여 감소한 양을 나타낸 결과이다. (b)는 안정화제 5% 혼합비율을 기준으로, 기계혼합방법과 생물혼합방법을 대조하였다. 28일간 노출된 Lumbriculus variegatus의 체내 축적 감소량은 생물혼합이 84.8%, 기계혼합이 76.8% 감소하였다. (c)는 안정화제 10% 혼합비율을 기준으로 기계혼합 방법과 생물혼합 방법을 대조하였다. 28일간 노출된 Lumbriculus variegatus의 체내 축적 감소량은 기계혼합이 84.8%, 생물혼합이 72.3% 감소하였다.
3.3 수중용출량 분석
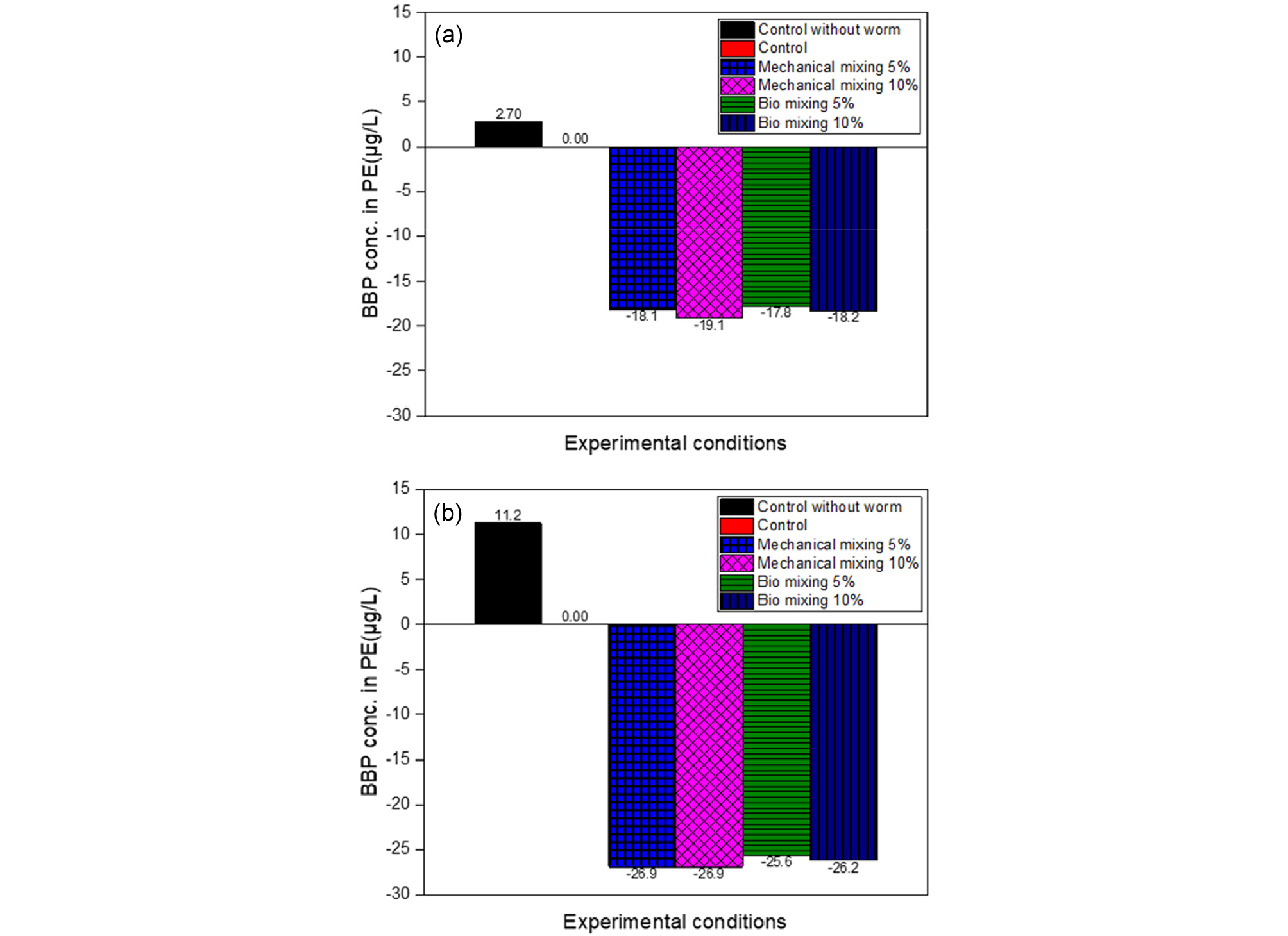
Fig. 6은 수중으로 용출되는 BBP의 농도를 원형으로 자른 LDPE를 이용하여 흡착한 뒤 분석한 결과 그래프이다. (a)는 control의 값을 기준으로 하고, 실험군들의 결과를 상대적으로 비교하여 안정화제의 안정화량을 비교 및 분석하였다. Control에 비해 모든 그래프가 적게 측정이 된 것을 확인할 수 있다. 이는 기계혼합의 경우에는 안정화제 혼합비율 및 혼합방법에 따른 안정화 정도를 상대적으로 비교하였다. (a)는 7일, 14일, 21일, 28일간의 노출 기간 후 분석한 원형 LDPE 데이터를 시각화한 그래프이다. 분석 결과 기계혼합 10% 실험군이 19.1% 더 저감 된 것으로 측정되었고, 그 뒤로 생물혼합 10%(18.2%), 기계혼합 5%(18.1%), 생물혼합 5%(17.8%) 순서로 저감 되었다.
(b)는 28일간의 노출 기간 후 분석한 원형 LDPE를 분석한 뒤, control의 결과를 기준으로 용출량 차이를 시각화한 그래프이다. 이에 따르면 기계혼합 10%(26.92%)가 기계혼합 5%(26.91%) 보다 0.01% 더 근소한 차이로 높은 안정화율을 보이고 있으며, 그 뒤로 생물혼합 10%(26.2%), 생물혼합 5%(25.6%)가 control보다 더 저감 되었다. 상대적으로 더 높은 용출량을 보인 생물혼합은 생물 교란에 의해 아래의 토양으로부터 유기오염물질이 용출되어(Kupryianchyk et al., 2013) Fig. 6과 같은 결과를 보인 것으로 판단된다.
3.4 공극수 농도 분석
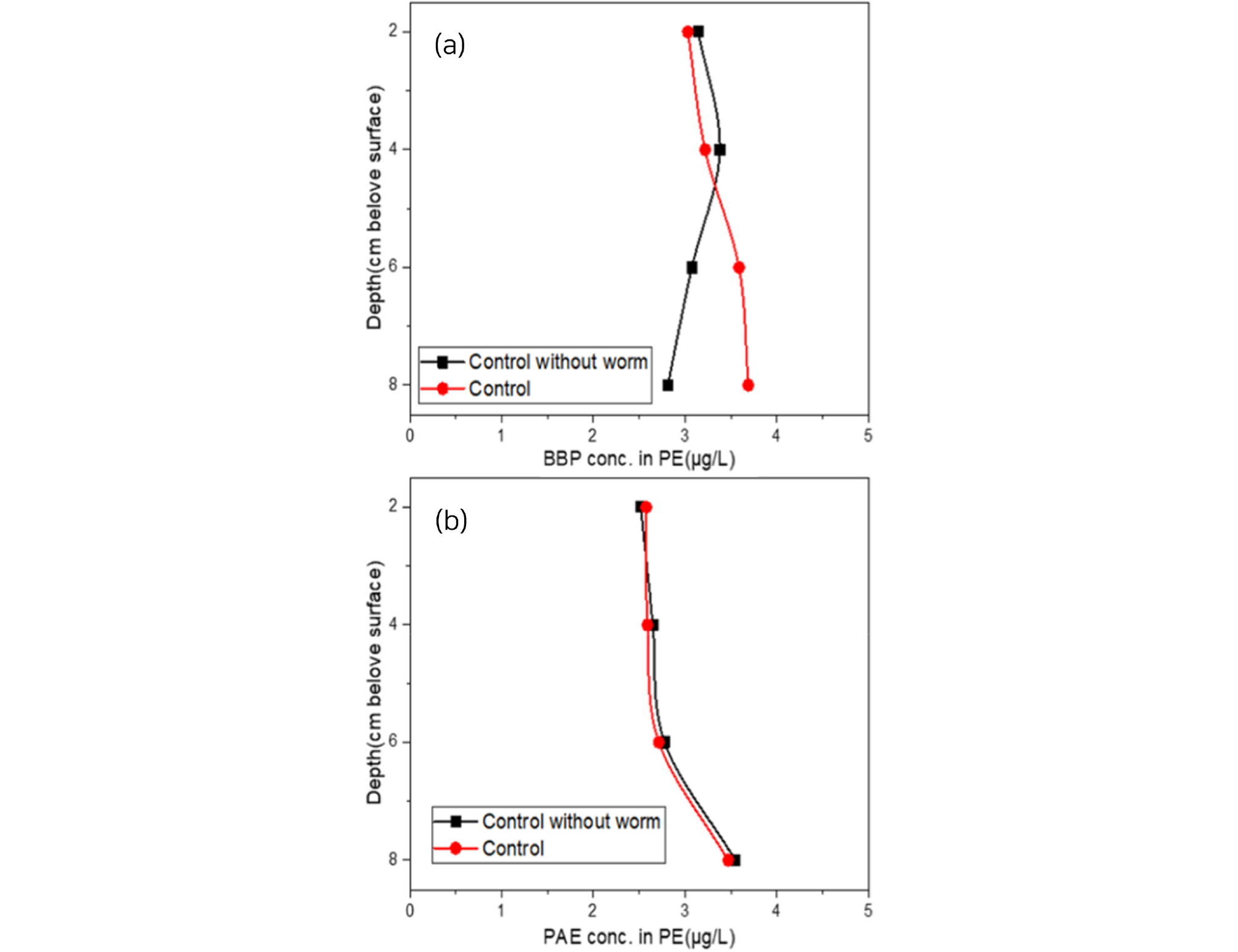
노출 기간 7일 후 측정한 (a)와 노출 기간 28일 후 측정한 (b)의 Lumbriculus variegatus가 많이 분포하는 0~4cm의 측정값은 control을 control without worm으로 나누고 백분율을 구한 후 0~2cm의 값과 0~4cm의 값의 평균을 구하여 비교하였다. 실험 기간 7일과 28일간의 그래프를 비교하였다. 생존률 평가실험 진행 중 Lumbriculus variegatus의 주 서식 범위가 0~4cm임을 확인하였다. 따라서 Lumbriculus variegatus의 유무에 따른 영향을 분석하기 위해 0~4cm 범위의 BBP 평균 축적량을 비교하였다. Fig. 7은 Lumbriculus variegatus에 의해 발생할 수 있는 공극수의 BBP 농도변화 영향을 확인하기 위해 control과 control without worm을 비교한 그래프 결과이다. 그 결과 (a)의 0~4cm 값은 control이 control without worm보다 4% 더 높은 축적량을 보였으며, (b)의 0~4cm 값은 control이 control without worm보다 0.2% 더 낮은 축적량을 보였다. (a)는 Lumbriculus variegatus의 활발한 활동으로 인해 부유 BBP가 상승하여 control without worm에 비해 4~8cm 구간은 낮은 농도로, 0~4cm 구간은 높은 농도로 측정이 되었다(Kupryianchyk et al., 2013). (b)는 시간이 지남에 따라 안정화가 진행되었고, BBP가 토양에 흡착 및 축적되며 L 형태의 그래프를 나타내었을 가능성이 있고, 공극수가 상등수에 희석되면서 표면에 가까울수록 BBP 농도가 줄어들었기 때문일 가능성 또한 존재한다(Lin et al., 2014). 7일에서는 control without worm을 기준으로 control이 4.2% 더 많이 축적되었고, 28일에서는 0.1% 덜 축적되었다. 이를 통해 Lumbriculus variegatus의 존재가 미미한 영향을 유발할 수 있으나, 결과적으로 0.1%의 차이를 보이기에 미미한 영향만이 존재할 것으로 예상된다. 이에 Lumbriculus variegatus에 의한 영향은 없다고 판단하고 분석을 진행하였다.
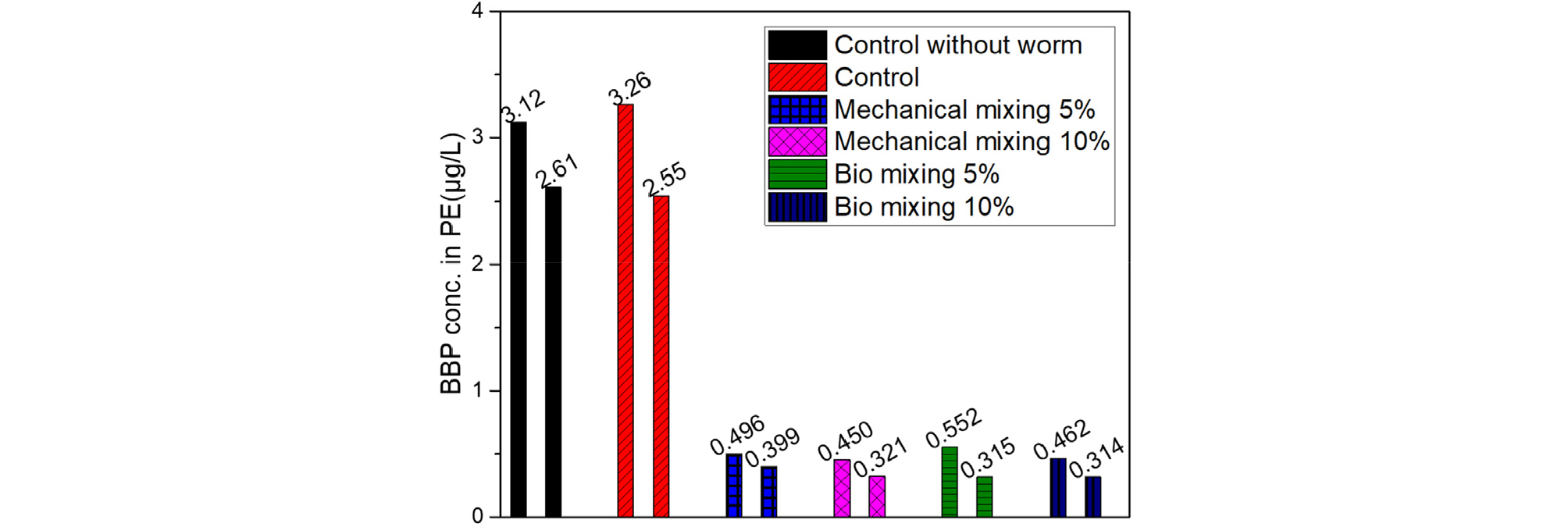
Fig. 8은 LDPE를 이용하여 토양 공극수 내의 유기오염물질 농도를 분석한 그래프이다. 본 실험의 최종 목표 기간인 28일 후의 안정화제 효율 평가를 진행하기 위해서 7일간 측정한 결과값과 28일간 측정한 결과값의 공극수 농도 분석 결과 그래프를 비교하였다. 왼쪽에 위치한 막대그래프가 노출 기간 7일간 측정한 공극수 농도이며 오른쪽에 위치한 막대그래프가 노출기간 28일간 측정한 공극수의 농도를 나타낸 그래프이다. 비교는 7일간 측정한 결과값을 기준으로 28일간 측정한 결과값의 저감 정도를 비교하였다. 노출 기간 7일 결과 중 control과 Lumbriculus variegatus가 없는 실험군 비교 시, control보다 Lumbriculus variegatus가 없는 실험군이 약 4% 더 저감된 결과를 나타내었다. 이는 Lumbriculus variegatus의 활동에 의해 토양이 교란되어 BBP가 공극수에 더 축적된 것에 의해 나타난 결과라고 판단된다. Control과 기계혼합 5%, 기계혼합 10%, 생물혼합 5%, 생물혼합 10% 비교 시, 각각의 저감 정도는 약 84.8%, 86.2%, 83.1%, 85.8% 저감된 결과를 나타내었다. 모든 안정화제 혼합 실험군에서 80% 이상의 저감이 확인되었으며, 기계혼합의 안정화율이 평균적으로 약 0.5% 더 높은 저감 효율을 보였다. 노출 기간 28일 결과 중 control과 Lumbriculus variegatus가 없는 실험군 비교 시, Lumbriculus variegatus가 없는 실험군보다 control이 약 2% 더 저감된 결과를 나타내었다. 이는 일부 BBP가 Lumbriculus variegatus의 활동에 의해 축적된 것(Wang et al., 2023)에 의해 나타난 결과라고 판단된다. Control과 기계혼합 5%, 기계혼합 10%, 생물혼합 5%, 생물혼합 10% 비교 시, 각각의 저감 정도는 약 84.4%, 87.4%, 87.6%, 87.7% 저감된 결과를 나타내었다. 모든 안정화제 혼합 실험군에서 80% 이상의 저감이 확인되었으며, 생물혼합에서 평균적으로 약 1% 더 높은 저감 효율을 보였다. 두 실험 기간의 비교 결과 0.5%에서 1% 사이라는 작은 저감 효율 차이를 보였다.
4. 결 론
본 연구에서는 산/염기 개질활성탄을 안정화제로 이용하여 유기오염물질인 BBP에 오염된 퇴적토의 안정화 실험을 진행하였다. 샘플은 개질활성탄을 혼합하지 않은 샘플과 개질활성탄 혼합농도를 5%와 10%로 구분한 샘플, 동일한 혼합농도를 가지지만 다른 혼합방법을 적용한 샘플로 구분하였다. 개질활성탄을 혼합하지 않은 샘플은 Lumbriculus variegatus존재 유무에 따라 구분하여 6가지의 샘플을 제작하였다. 용출수와 공극수, Lumbriculus variegatus 체내의 BBP 축적 농도를 분석하였고, Lumbriculus variegatus의 생존율을 측정하는 실험을 수행하였다.
모든 샘플의 Lumbriculus variegatus 생존율은 90% 이상의 수치를 보이며 안정적인 생존율을 나타내었다(OECD., 2004). 체내 BBP 축적농도는 10% 혼합비율을 적용한 실험군보다 5% 혼합비율을 적용한 실험군이 2% 더 낮은 농도로 검출되며 높은 안정화 효과를 나타내었다. 용출수의 BBP 농도는 모든 노출 기간의 평균값 비교 결과 기계혼합 10%의 안정화가 가장 높게 분석되었으나, 가장 낮은 안정화를 보인 생물혼합 5%와 1.3%라는 큰 차이를 보이지 않았다. 노출 기간 28일의 샘플값 비교 결과 모든 기계혼합 실험군의 안정화가 가장 높게 나타났으며, 가장 낮은 안정화를 보인 생물혼합 5%와 1.3%라는 큰 차이를 보이지 않았다. 공극수의 농도는 노출기간 7일 후 결과 비교와 노출기간 28일 후 결과 비교를 통해 안정화 효율을 판단하였다. 노출기간 7일 후의 결과는 기계혼합 실험군에서 생물혼합 실험군보다 높은 안정화율을 보였으며, 약 1% 차이로 10%를 혼합한 기계혼합 실험군이 5%를 혼합한 기계혼합 실험군보다 높은 안정화율을 보였다. 노출기간 28일 후의 결과는 생물혼합 실험군이 기계혼합 실험군보다 높은 안정화율을 보였으며, 약 0.1% 차이로 10%를 혼합한 실험군이 5%를 혼합한 실험군보다 높은 안정화율을 보였다. 조건에 따른 안정화 효율의 차이는 있었으나 그 차이가 3% 미만이며 모든 안정화 효율은 80% 이상을 나타내었다.
활성탄은 저서생물의 활동에 있어 성장에 관련된 영향은 주지만 생존에는 큰 영향이 없는 것으로 확인하였으며, 본 실험의 결과 또한 OECD의 기준에 따라 모든 조건에서 90% 이상의 생존율을 보였기에 안정화제에 의한 생존율 변화는 없는 것으로 판단하였다. 용출수 오염농도와 공극수 오염농도 측정결과를 종합한 결과 두 결과에서 우수한 안정화 성능을 보이는 혼합방법과 혼합비율이 다르게 나타났다. 다만, 그 차이는 1%~3%로 미미하며 활성탄의 혼합비율이 증가할수록 퇴적토 내부의 영양물질이 흡착되어 저서생물에 영향을 끼칠 수 있기에 5% 혼합비율을 선정하는 것이 합당하다는 판단을 하였다. 전체적인 퇴적토 환경을 보았을 때, 기계혼합을 진행하여도 그 한계로 인해 깊은 위치에 존재하는 토양은 혼합이 이루어지기 어려워 본 실험에서 진행한 생물혼합의 상태와 유사한 조성이 이루어지므로 생물혼합의 조건 또한 구현할 수 있다고 판단되며 생물혼합에 의한 혼합한계 또한 존재하므로 기계혼합 방식의 5% 안정화제 혼합이 본 실험 목표에 적합한 방법이라고 판단된다. 본 논문을 통해 현재 국내 퇴적물 정화방법의 다양성 및 개선방법에 대한 긍정적인 영향이 미칠 수 있을 것으로 판단된다.
본 연구는 안정화제를 이용한 유기오염물질에 오염된 퇴적토 복원을 위한 정보를 제공한다.